Ab dem 07.06.2021 sollen die CoVid-19-Impfangebote ausgeweitet werden. Viele sind trotz zahlreicher Informationsmöglichkeiten aufgrund der kurzen Entwicklung und der verwendeten genetischen Impfstoffe verunsichert. Sind die Sorgen begründet?
Zu Gunsten der Verständlichkeit stark vereinfacht
Es wird befürchtet, dass langfristige Nebenwirkungen auftreten oder ein Einbau der genetischen Informationen in die Körperzellen möglich ist. Das Auftreten von Thrombosen bei dem Impfstoff von AstraZeneka wurde in den Medien aufgegriffen, zum Teil aber überbewertet. Die Nebenwirkungen schienen ein Hinweis darauf zu sein, dass vorab keine ausreichenden Studien stattfanden.
Im Folgenden sind einige Informationen zu Impfstoffen, Impfstoffentwicklung und -zulassung allgemein und bezogen auf die CoVid-19-Impfstoffe zusammengestellt. Aufgrund des Umfangs des Themas kann es sich hierbei nur um einen Überblick handeln. Jeweils detaillierte Aussagen zur Bewertung der Zulassungen und deren Eingangsdaten, zur Sicherheit der Impfstoffe, zu Vergleichen der Impfstoffe etc. ist in diesem Überblick nicht möglich. Seitens der offiziellen Stellen wird eine nahezu unüberschaubare Fülle von Informationen in unterschiedlicher fachlicher Tiefe zur Verfügung gestellt. Eine kleine Auswahl der Informationen ist unter Quellen und Informationsmöglichkeiten aufgeführt.
Hinweis: Die Daten werden i. d. R. in Prozent dargestellt, da dies eine „gewohnte“ Größe ist. Grundsätzlich ist bei Prozentzahlen immer die Bezugsgröße („Was ist 100 %“) relevant. Sofern dies nicht eindeutig aus dem Kontext hervorgeht, wird die Bezugsgröße angegeben.
Grundprinzip Impfungen: Aktivierung Immunsystem
Dringt ein Erreger in den Körper ein, wird das Immunsystem aktiviert. Im ersten Schritt wird der Erreger mit unspezifischen Abwehrzellen bekämpft. Im zweiten Schritt erfolgt eine auf den Erreger zugeschnittene Abwehrreaktion mit spezifisch gebildeten Antikörpern und der Bildung von Gedächtniszellen. Erneute spätere Infektionen können dadurch schnell bekämpft werden und führen zu keinen schweren Erkrankungen.
Erreger werden vom Immunsystem anhand ihrer Rezeptorproteine auf ihrer Oberfläche (Spikes) erkannt. Jeder Erregertyp hat (wie jede Zelle) spezifische Oberflächenproteine, die ihn von anderen Erregern und Zellen unterscheiden. Diese Proteine werden als Antigene bezeichnet.
Krankmachende Wirkung können sowohl die Erreger an sich haben, aber auch die von ihnen ausgeschiedenen Stoffwechselprodukte, die als Gifte (Toxine) wirken. Diese Toxine bestehen aus Proteinen und sind daher ebenfalls Antigene, die zur Bildung von Antikörpern führen.
Dieses Prinzip der Immunabwehr (Antigene werden durch spezielle Antikörper bekämpft) nutzt man bei Impfungen.
Vorteile von Impfungen
Impfungen haben individuelle und gesellschaftliche Vorteile. Impfungen:
- bieten nach einer Infektion einen individuellen Schutz vor der entsprechenden Erkrankung;
- schützen den Fötus vor entsprechenden Infektionen (z. B. Röteln);
- führen zu einer allgemeinen Aktivierung des Immunsystems (Daher wird während der Pandemie die Grippeschutzimpfung empfohlen, obwohl durch diese keine Antikörper gegen das Corona-Virus gebildet werden);
- bieten einen Herdenschutz, wenn ca. 80 % der Bevölkerung geimpft (oder genese Erkrankte) sind. Durch den Herdenschutz sind Personen, die sich aus gesundheitlichen Gründen nicht impfen lassen können oder bei denen die Impfung nicht wirksam ist, indirekt geschützt; hinsichtlich CoVid-19 ist das Erreichen eines Herdenschutzes (neben dem individuellen Schutz) ein wesentlicher Aspekt zur Aufhebung des Lockdowns und zur Wiederaufnahme des normalen wirtschaftlichen und gesellschaftlichen Lebens;
- können ggf. zur (regionalen) Ausrottung von Krankheiten führen, z. B. Pocken, Polio.
Nachteile von Impfungen
Jede Wirkung hat Nebenwirkungen. Wirkung und Nebenwirkung sollten in einem statistisch „akzeptablem“ Verhältnis stehen. Die Wirkung sollte statistisch sehr häufig auftreten, Nebenwirkungen selten, schwere Nebenwirkungen sehr selten oder gar nicht. Im statistischen Mittel bedeutet dies, dass Medikament / Impfung wirksam sind ohne nennenswerte und / oder gehäufte Nebenwirkungen. Bei einigen Personen treten jedoch Nebenwirkungen auf, bei sehr wenigen extreme Nebenwirkungen. Die Abwägung von Nutzen und Risiko ist Bestandteil der Zulassung sowie der Impfempfehlungen.
Wie oben dargestellt, reagiert der Körper mit einer Immunreaktion. Diese Immunreaktion fordert den Körper, sodass leichte Abgeschlagenheit auftreten kann. Daher sollte man sich grundsätzlich nach einer Impfung schonen.
Je nach Impfstoff und individueller Konstitution können durch den Impfstoff ähnliche, aber abgeschwächte, Symptome wie bei der eigentlichen Krankheit auftreten (Impfkrankheit). Diese treten nach der erregerspezifischen Inkubationszeit auf, verschwinden aber relativ schneller wieder.
Bei CoVid-19-Impfungen sind ein Großteil der Nebenwirkungen in diese Kategorien einzuordnen, z. B. Abgeschlagenheit, Kopfschmerzen, Fieber, Atembeschwerden.
Adjuvanzien (siehe unten) können zu Reaktionen an der Einstichstelle führen. Diese Nebenwirkungen treten meist nur kurzzeitig auf.
Bei CoVid-19-Impfungen sind zahlreiche Nebenwirkungen in diese Kategorie einzustufen.
Einteilung der Nebenwirkungen
Man kann Impfnebenwirkungen unter verschiedenen Gesichtspunkten betrachten: Die gängigsten sind Schwere, Häufigkeit und Vorhersagbarkeit.
Unabhängig von diesen Gesichtspunkten definiert das Infektionsschutzgesetz (IfSG) einen Impfschaden wie folgt:
„die gesundheitliche und wirtschaftliche Folge einer über das übliche Ausmaß einer Impfreaktion hinausgehenden gesundheitlichen Schädigung durch die Schutzimpfung; ein Impfschaden liegt auch vor, wenn mit vermehrungsfähigen Erregern geimpft wurde und eine andere als die geimpfte Person geschädigt wurde“.
Für Impfschäden ist auf Antrag eine finanzielle Entschädigung durch Bund / Land möglich (IfSG i. V. m. BVG).
Schwere
Nach der Schwere der Nebenwirkungen wird unterschieden zwischen Impfreaktionen und Impfkomplikationen.
Impfreaktion
Impfreaktionen sind relativ häufige, aber schwache Nebenwirkungen. Hierzu zählen leichte Schmerzen, Rötungen und Schwellungen an Einstichstelle. Aber auch (nach ca. 3 Tagen) leichte Temperaturerhöhung, Unwohlsein, Gefühl von Schlappheit für 1 – 2 Tage.
Bei allen COVID-19-Impfstoffen treten (in unterschiedlicher Häufigkeit) Nebenwirkungen wie Schwellungen und / oder Schmerzen an der Injektionsstelle, lokale Reaktionen und Ermüdungen auf. Diese Symptome sind vor allem bei dem Impfstoff von BioNTech feststellbar.[1]
Es treten auch typische Krankheitssymptome (Impfkrankheit), wie Kopfschmerzen, grippeähnliche Erkrankung, Schüttelfrost, Fieber, auf. Diese Symptome wurden vor allem beim Impfstoff von AstraZeneka festgestellt.[1]
Impfkomplikation
Impfkomplikationen (Impfzwischenfälle) sind seltene, aber schwere Erkrankungen, die sich ursächlich auf die Impfung zurückführen lassen. Diese Nebenwirkungen sind meldepflichtig.
Ziel der Zulassung von Impfstoffen und deren Überwachung nach der Zulassung (siehe unten) ist u. a. die Überprüfung, dass Impfkomplikationen in keinem Verhältnis zur Schwere und Häufigkeit der Krankheit, gegen die geimpft wurde, stehen.
Beispiel: Bei einer Masernerkrankung kann mit einer Wahrscheinlichkeit von 1:10.000 eine Hirnhautentzündung auftreten. Durch eine Masernimpfung kann ebenfalls eine Hirnhautentzündung auftreten, allerdings mit einer Wahrscheinlichkeit von 1:1.000.000.
Bei dem AstraZeneka-Impfstoff wurden bis zum 11.04.2021 sehr seltenThrombosen mit Thrombozytopenie (Thrombosen mit Thrombozytopenie-Syndrom = TTS) gemeldet. Je nach Altersgruppe und Geschlecht betrug der Anteil 0,2 – 2,2 Fälle je 100.000 Impfdosen (entspricht: 0,0002 – 0,0022 %). Allerdings geht man von einer höheren Dunkelziffer aus. In Dänemark wurde ein hoher Frauenanteil geimpft. Hier betrug die Thromboserate (nicht TTS) 0,011 % (bzw. 11 Fälle auf 100.000), inkl. 2,5 Sinusvenenthrombosen je 1.000.000 Impfdosen.
Da in den USA bei dem Vektorimpfstoff von Janssen ähnliche Fälle festgestellt wurden, sind diese Nebenwirkungen in die Produktinformationen eingeflossen.
Häufigkeit
Unterteilt nach der Häufigkeit des Auftretens wird unterschieden:
- sehr häufig: größer beziehungsweise gleich 1/10, entspricht 10 %,
- häufig: größer beziehungsweise gleich 1/100 bis kleiner 1/10, entspricht 1 – 10 %,
- gelegentlich: größer beziehungsweise gleich 1/1.000 bis kleiner beziehungsweise gleich 1/100, entspricht 0,1 – 1 %,
- selten: größer beziehungsweise gleich 1/10.000 bis kleiner beziehungsweise gleich 1/1.000, entspricht 0,01 – 0,1 %,
- sehr selten: kleiner beziehungsweise gleich 1/10.000, entspricht < 0,01 %.
Die festgestellten Nebenwirkungen der zugelassenen CoVid-19-Impfstoffe sind den Produktinformationen zu entnehmen (siehe Informationsmöglichkeiten – Informationen zu den Impfstoffen – Produktinformationen).
Vorhersehbarkeit
Neben den o. g. Unterteilungen kann man auch unterscheiden zwischen
- vorhersehbaren Nebenwirkungen: z. B. Reaktionen an der Impfstelle, Impfkrankheiten,
- unvorhersehbare Nebenwirkungen: Nebenwirkungen, die aus wissenschaftlicher Sicht nicht zu erwarten sind und erst in den klinischen Phasen oder in den Postmarketing-Studien festgestellt werden können.
Bei Reizungen etc. an der Einstichstelle handelt es sich um vorhersehbare Nebenwirkungen. Die TTS nach den Impfungen von AstraZeneka ist eine unvorhersehbare Nebenwirkung.
Home // Seitenanfang // Alle Beiträge Naturwissenschaft
Langzeitschäden / -wirkungen
Bleibende Schäden nach einer Impfung stellen definitionsgemäß keine Langzeitschäden dar, sondern sind Impfschäden.
Langzeitschäden können entstehen, wenn Medikamente über längere Zeit eingenommen werden. Sie können teilweise erst Jahre nach Beginn der Einnahme auftreten.
Im Gegensatz zu dauernd / häufig eingenommenen Medikamenten erfolgen Impfungen nur sehr selten (1 – 2 X oder im Abstand von mehreren Jahren) und bewirken eine unmittelbare Reaktion im Körper (Aktivierung Immunsystem). Im Gegensatz zu Medikamenten werden Impfstoffe nicht verstoffwechselt, sondern regen das Immunsystem an. Eine Speicherung des Impfstoffes erfolgt nicht. Langzeitschäden sind daher bei Impfungen nicht oder nur sehr selten zu erwarten.
Als Langzeitschaden kann die Narkolepsie bei der Grippeschutzimpfung 2008/09 (Impfstoff Pandemrix) angeführt werden. Narkolepsie ist eine Schlaf-Wach-Störung, die häufig als „Schlafkrankheit“ bezeichnet wird und autoimmune Ursachen hat. Häufig wurden die Fälle bereits innerhalb von 3 Monaten nach der Impfung registriert (Nebenwirkungen), sehr selten erst später (Langzeitschäden oder verspätet erkannte und gemeldete Nebenwirkungen). Insgesamt betrug das Risiko rd. 0,005 % (bezogen auf die Anzahl der Impfungen). [2]
Indirekte Effekte durch Impfungen
Neben individuellen Nachteilen können übergreifende Nachteile auftreten.
- Verschiebung der Krankheitslast: Durch Impfungen bestimmter Personengruppen können Erkrankungen in anderen Personengruppen häufiger auftreten. Z. B. können Kinderschutzimpfungen dazu führen, dass die Erkrankungen bei älteren Menschen ohne Impfschutz vermehrt auftreten (z. B. bei Masernimpfungen).
- Fehlende Booster-Infektionen („Auffrischung“ des Immunitäts-Status durch wiederholten Kontakt mit dem Erreger): Aufgrund der niedrigen Virenlast in der Bevölkerung fehlt regelmäßiger Erregerkontakt (z. B. nach Varizella-zoster-Impfungen)
- Auftreten von Erregervarianten, die nicht vom Impfstoff erfasst werden (z. B. Pneumokokkenimpfung).
Argumente gegen das Impfen
Durch Impfungen konnten viele Krankheiten eingedämmt werden. Dies führt dazu, dass die Häufigkeit und Schwere dieser Erkrankungen in Vergessenheit gerät und eine Impfmüdigkeit in der Bevölkerung auftritt.
Impfgegner bewerten die Nachteile von Impfungen überproportional hoch gegenüber deren Vorteilen oder ziehen als Vergleichsbasis das (aufgrund der Impfungen) seltene Auftreten der schweren Erkrankungen heran. Durch Ungeimpfte können diese Krankheiten jedoch wieder auftreten oder eingeschleppt und verbreitet werden (Bsp. Masern, Diphterie).
Nicht selten werden Argumente gegen das Impfen mit zusätzlichen pseudowissenschaftlichen Angaben und Verschwörungstheorien verknüpft. Studien werden völlig ignoriert oder nur auszugsweise mit ins Konzept passenden Aussagen oder willkürlichen Interpretation zitiert. Es ist ein zentrales Element von Verschwörungstheorien, offizielle Aussagen (inkl. Berichte der „obrigkeitshörigern“ Medien) als unvollständig, manipuliert und falsch darzustellen. Eine Auseinandersetzung auf wissenschaftlicher Ebene ist mit Verschwörungstheoretikern daher nicht möglich.
Von zahlreichen möglichen Beispielen nur eines:
Auf der Seite „Impf-Info.de“ (nicht zu verwechseln mit der Seite des BZgA: impfen-info.de) steht in einem Artikel, in dem der Herdenschutz bei CoVid-19-Erkrankungen angezweifelt wird [3]:
„Die bisher mit Abstand aussagekräftigste Studie zur Frage des Übertragungsrisikos nach Impfung stammt von Public Health England (Harris 2021): hier wurden in mehr als 300.000 Haushalten das Risiko verglichen, sich bei einem infizierten Haushaltsmitglied („index case“) anzustecken, wenn dieses entweder ungeimpft war oder mindestens 21 Tage zuvor entweder Vaxzevria® oder Comirnaty® erhalten hatte. Das Ergebnis ist ernüchternd: „These results show that the likelihood of household transmission is 40-50% lower for households in which the index cases are vaccinated 21 days or more prior to testing positive (compared to no vaccination), with similar effects for both ChAdOx1 nCoV-19 and BNT162b2 vaccines.“ – das Risiko der Übertragung auf andere wurde nicht einmal halbiert…“
In der Literaturliste des Artikels ist die Studie nicht aufgeführt. Link zur Studie: „Impact of vaccination on household transmission of SARS-COV-2 in England“.
Ziel der Studie war es, zu ermittelt, ob Personen, die nur eine Impfdosis erhalten haben, aber dennoch innerhalb von 60 Tagen an CoVid-19 erkranken, für ihre Haushaltsmitbewohner ein geringeres Infektionsrisiko darstellen. Demzufolge hatten 93 % der Studienteilnehmer lediglich die erste Impf-Dosis erhalten. Die Studie belegt also, dass bereits eine erste Impfung die Übertragbarkeit reduziert.
In den Zulassungsinformationen der in der Studie verwendeten Impfstoffe ist hinsichtlich des Eintrittes des Impfschutzes zu lesen (s. Informationen zu den Impfstoffen – Produktinformationen):
Astrazeneka (ChAdOx1): „Der Schutz setzt ungefähr 3 Wochen nach der ersten Vaxzevria-Dosis ein. Personen sind möglicherweise bis 15 Tage nach Gabe der zweiten Dosis nicht vollständig geschützt.“
BioNTech (BNT162b2): „… Personen sind möglicherweise erst 7 Tage nach ihrer zweiten Impfdosis vollständig geschützt.“
Nach 21 Tagen ist demnach nach der ersten Impfung bei keinem der Impfstoffe ein vollständiger Impfschutz zu erwarten.
Das auf der Webseite verwendete Zitat ist in der Studie zu Beginn der Diskussion der Ergebnisse zu finden. Es stellt die Ergebnisse dar, die im weiteren Verlauf der Diskussion bewertet werden – und zwar im Hinblick auf reduzierte Infektionsgefahr für Dritte nach der ersten Impfung der Probanden.
Ziel und Kernaussage der Studie stehen also im krassen Gegensatz zu der auf der Webseite suggerierten Aussage. Insbesondere lässt diese Studie keinen Schluss über Herdenschutz nach vollständiger Impfung zu.
Von den Personen, die Impfungen vergessen, deren Relevanz falsch einstufen oder auf Basis falscher Aussagen gegen Impfungen argumentieren, sind jene Personen abzugrenzen, die sich aufgrund individueller gesundheitlicher Gründe gegen Impfungen entscheiden (müssen).
Impfstoffe
Man unterscheidet zwischen passiven und aktiven Impfungen. Im Folgenden wird nur auf aktive Impfungen eingegangen.
Bei passiven Impfungen werden dem Körper fertige Antikörper, die in anderen Organismen gebildet wurden, zugeführt. Diese Antikörper „fangen“ wie die körpereigenen Antikörper, die Krankheitserreger (Antigene) ab. Im Gegensatz zu aktiven Impfungen wirken sie sofort. Passive Impfungen schützen nur solange, wie sich die Antikörper im Körper befinden, es werden keine Gedächtniszellen gebildet. Bei einer Halbwertzeit von 3 Wochen besteht nach ca. 2 – 3 Monaten kein Schutz mehr.
Passive Impfungen werden hauptsächlich dann eingesetzt, wenn eine aktive Impfung aus Zeitgründen nicht mehr möglich ist, z. B. nach einer erfolgten Infektion.
Eine natürliche „passive Impfung“ erhält der Embryo bereits in der Plazenta von der Mutter und das Neugeborene über die Muttermilch (Nestschutz).
Aktive Impfung werden auch als Schutzimpfung bezeichnet. Die erfolgten Schutzimpfungen sind im „Impfpass“ einzutragen.
Die Impfstoffe für Schutzimpfungen unterscheiden sich deutlich von anderen Arzneimitteln:
- sie werden zur Prävention von Infektionskrankheiten eingesetzt,
- sie werden bei gesunden Menschen zum Schutz vor Erkrankungen eingesetzt,
- sie bieten langzeitigen Schutz, müssen also nicht ständig wiederholt werden. Ausnahmen stellen Impfstoffe gegen sich verändernde Erreger dar, bei denen die Impfstoffe kontinuierlich an die Erreger angepasst werden (z. B. Grippeschutzimpfung).
Das Grundprinzip ist bei allen Impfungen gleich: Impfstoffe sind immunmodulierende Substanzen, die eine Infektion vortäuschen. Der Körper reagiert auf die Impfung (das Antigen, z. B. den Erreger) mit einer Immunantwort – er bildet Antikörper und Gedächtniszellen. Wie bei einer echten Infektion kann der Körper bei einem späteren realen Kontakt mit dem Erreger sehr schnell reagieren, sodass Krankheitssymptome nicht oder nur in geringem Umfang auftreten. Der Aufbau des Impfschutzes benötigt einige Zeit, da der Körper die speziellen Antikörper zunächst bilden muss.
Bei einem Impfversagen werden keine Antikörper gebildet und es ergibt sich somit kein Schutz. Impfversagen ist relativ selten, die genauen Ursachen sind unbekannt. Häufig ergibt sich der gewünschte Impfschutz bei einer Wiederholungsimpfung.
Impfstoffe können in verschiedene Gruppen eingeteilt werden.
Lebendimpfstoffe
Bei Lebendimpfstoffe werden abgeschwächte Erreger geimpft, die sich zwar im Körper vermehren, aber keine schweren Erkrankungen erzeugen können. Als Impfnebenwirkung (siehe oben) kann die Krankheit jedoch in stark abgeschwächter Form auftreten (Impfkrankheit, siehe oben).
Durch Lebendimpfstoffe wird die beste Immunantwort erreicht. Sie dürfen allerdings nicht bei Menschen mit Immunschwäche verwendet werden.
Beispiele: Impfungen gegen Masern, Mumps, Röteln, Typhus.
Totimpfstoffe, inaktivierte Produkte
Bei diesem Impfstofftyp werden inaktive Erreger oder Teilprodukte, wie inaktivierte Bestandteile oder inaktivierte Stoffwechselprodukte des Erregers (z. B. Toxine), zugeführt.
Beispiele: Impfungen gegen FSMA, Polio, Typhus, Pneumokokken, Meningokokken, Influenza, Tetanus, Diphtherie.
Home // Seitenanfang // Alle Beiträge Naturwissenschaft
RNA- / DNA-Impfstoffe
Teilweise werden diese Impfstoffe auch als genetische oder genbasierte Impfstoffe bezeichnet.
Bei diesen Impfstoffen werden keine immunaktivierenden Substanzen (Antigene) des Erregers geimpft, sondern über die RNA / DNA die Information zur Herstellung der speziellen Antigene: In den Körperzellen wird aus den im Impfstoff enthaltenen Informationen (RNA / DNA) das Antigen produziert, welches den Körper zur passenden Immunantwort veranlasst.
Ein wesentlicher Vorteil dieser Impfstoffe ist, dass das grundsätzliche Verfahren (Einbringen der Oberflächen-Struktur mittels RNA / DNA) unabhängig vom Erreger ist. Bei Auftreten veränderter (oder neuer) Erreger kann somit relativ schnell ein geeigneter Impfstoff produziert werden.
Es wird (in Bezug auf CoVid-19-Impfstoffen) unterschieden zwischen mRNA-Impfstoffen und Vektor-Impfstoffen.
mRNA-Impfstoffe: Die Information für die Bildung der spezifischen Oberflächenstruktur (Antigenstruktur, Spike) der krankmachenden Viren wird über die mRNA in die Körperzellen injiziert.
mRNA (messenger-RNA) „bringt“ in der normalen Körperzelle die Informationen von der DNA aus dem Zellkern in die Zelle, sodass die entsprechenden Proteine produziert werden können. Die fremde mRNA aus der Impfung wird genauso „verarbeitet“ wie die zelleigene mRNA, dass heißt, es werden die auf dem Bauplan der mRNA codierten Proteine produziert.
Im Fall der CoVid-19-Impfstoffe handelt es sich bei den produzierten Proteinen um die Oberflächenstruktur (Spike = Antigen) des Corona-Virus, die zur Antikörperbildung führt.
Da die mRNA sehr instabil ist, müssen Zusatzstoffe (Adjuvanzien, siehe unten) eingesetzt werden, die die mRNA vor vorzeitigem Zerfall schützen.
Die beiden Corona-Impfstoffe von BioNTech und Moderna sind die ersten zugelassenen mRNA-Impfstoffe. Die mRNA ist zum Schutz in Lipidnanopartikel eingehüllt.
Vektor-Impfstoffen: Die Erbsubstanz eines gut untersuchten, aber harmlosen (und / oder inaktivierten) Virus wird genetische verändert, sodass sie den Bauplan für die Oberflächenproteine des Erregers enthält. Es werden 2 Varianten unterschieden:
- Nicht vermehrungsfähige Viren: Die Information für die Bildung der spezifischen Oberflächenstruktur (Antigenstruktur) der krankmachenden Viren wird über ein Virus in die Körperzellen eingeschleust. Die Zelle produziert daraufhin die Oberflächen-Antigene, die im Körper zur Bildung der spezifischen Antikörper führen. Der Vektor-Virus selbst wird nicht gebildet. Diese Impfstoffe können unter Totimpfstoffe eingeordnet werden.
- Vermehrungsfähige Viren: In der Virushülle ist eine Oberflächenstruktur des krankmachenden Virus enthalten. Das gesamte modifizierte Virus wird in den Körperzellen produziert und führt im Körper zur Antikörperbildung gegen das Virus, speziell gegen die Oberflächenstrukturen des Zielvirus. Bei diesen Impfstoffen handelt es sich um Lebendimpfstoffe (auch wenn Viren nicht als Lebewesen eingestuft werden).
Erste Erfahrungen mit diesen Impfstoffen konnten im Rahmen von Ebola-, MERS- und SARS-Epidemien gesammelt werden. Der Ebola-Impfstoff wurde 2019 zugelassen.

Die Corona-Impfstoffe von AstraZeneca und Janssen sind Vektorimpfstoffe. Über nicht vermehrungsfähige Viren (Adenovirus) wird die Information zur Bildung der Oberflächenproteine eingeschleust. Der Janssen-Impfstoff verwendet das Virus AD16, der AstraZeneka-Impfstoff ein von Schimpansen-Adenoviren abgeleitetes Virus (ChAdY25).
Adeno-Viren sind DNA-Viren, die in zahlreichen genetischen Varianten, darunter 7 für den Menschen pathogenen Formen (u. a. Erkältung), auftreten.
Hinsichtlich der Befürchtung, dass die DNA der Viren in die DNA der Körperzellen eingebaut wird, schreibt die Bundeszentrale für gesundheitliche Aufklärung (BZgA):
Mit Adenoviren – „Schnupfenviren“ – hat der menschliche Körper regelmäßig Kontakt. Auch bei natürlicher Infektion mit Adenoviren wurde bisher keine genetische Veränderung menschlicher Zellen beobachtet. Adenovirale Vektoren sind generell nichtintegrierende Vektoren, das heißt, sie bauen ihr Erbgut nicht in das menschliche Erbmaterial ein.
Das Genom der COVID-19-Vektorimpfstoffe auf Basis nicht vermehrungsfähiger Adenoviren verbleibt ebenso wie das anderer Adenoviren außerhalb der menschlichen DNA im Zellkern infizierter Zellen. Auch vor dem Hintergrund, dass sich die adenoviralen Vektoren aufgrund genetischer Veränderungen bei Geimpften nicht vermehren können und schnell vom Körper abgebaut werden, besteht nach dem aktuellen Stand der Wissenschaft kein Risiko des Einbaus der Adenovirus-Vektor-DNA in das menschliche Erbgut.
Bei Vektor-Impfstoffen kann eine vektorspezifiche Immunantwort auftreten: Hatte der Körper bereits Kontakt mit dem Vektorvirus reagiert er entsprechend auf den Vektor und die gewünschte Immunisierung gegen den Erreger bleibt aus oder wird verringert. Daher werden zum Teil bei der ersten und zweiten Impfung unterschiedliche Vektorviren verwendet.
Bei Vektor-Impfstoffen kann eine vektorspezifiche Immunantwort auftreten: Hatte der Körper bereits Kontakt mit dem Vektorvirus reagiert er entsprechend auf den Vektor und die gewünschte Immunisierung gegen den Erreger bleibt aus oder wird verringert. Daher werden zum Teil bei der ersten und zweiten Impfung unterschiedliche Vektorviren verwendet.
Bei dem Impfstoff von Janssen ist nur eine Impfung erforderlich. Der Impfstoff von AstraZeneka verwendet einen abgeleiteten Adenovirus-Typ (ChAdY25, s.o.).
Zusätze
Bei Totimpfstoffen ist, im Gegensatz zu Lebendimpfstoffen, die Zugabe von Hilfsstoffe (Adjuvanzien) erforderlich. Hierbei handelt sich um immunologisch wirksame Moleküle oder makromolekulare Komplexe, die Quantität, Qualität und Dauer der Immunantwort auf die Impfung verbessern sollen.
Man unterscheidet Vehikel / Carrierstoffe, die ein Depot für die Impf-Antigene darstellen und Substanzen, die immunstimulierend wirken.
Zu den häufig kritisierten Adjuvanzien zählen z. B. Aluminiumsalze. Sie sollen einen Depoteffekt über eine kontinuierliche Abgabe sowie eine erleichterte Aufnahme der Antigene bewirken. Der durch Impfungen zugeführte Aluminiumanteil liegt deutlich unterhalb des durch die Nahrung aufgenommenen Anteils.
Für lokale Reaktionen an der Einstichstelle der Impfung sind häufig diese Adjuvanzien verantwortlich. Die Nebenwirkungen (siehe oben) treten meist nur kurzzeitig auf.
Auch bei den CoVid19-Impfstoffen werden Adjuvanzien verwendet. mRNA-Impfstoffe verwenden Lipidnanopartikel zur Stabilisierung der mRNA.
Vektorviren können ebenfalls unter Adjuvanzien eingestuft werden.
Phasen der Zulassung von Impfstoffen
Entwicklung neuer Impfstoffe
Die Entwicklung von Impfstoffen ist kosten- und zeitintensiv. Nach Wiedemann [4] dauert die Impfstoffentwicklung in der Regel rd. 15 – 20 Jahre und kostet rd. 300 – 800 Millionen Euro (oder mehr). Ein großer Teil der Kosten ist für die Sicherheitsstudien erforderlich (mind. 300 Millionen Euro).
Der Erfolg – ein vermarktbarer Impfstoff – ist zu Beginn der Impfstoffentwicklung in der Regel sehr unsicher. Von 10.000 möglichen Stoffen aus der Forschung gelangen nur ca. 250 in die präklinische Phase und nur ca. 5 in die klinische Phase.
Firmen mit potenziell erfolgreichen Impfstoffkonzepten für CoVid-19-Impfungen erhielten umfangreiche Zuschüsse aus staatlichen und anderen Organisationen. Damit konnten die Firmen ihr Kostenrisiko hinsichtlich Fehlentwicklungen reduzieren, sowie Forschungs- und Produktionskapazitäten aufstocken.
Home // Seitenanfang // Alle Beiträge Naturwissenschaft
Phasen der Entwicklung
Präklinische Phase
Diese Phase kann bis zu 6 Jahren dauern. In dieser Phase werden die Substanzen an Zellkulturen und an geeigneten Tieren u. a. hinsichtlich ihrer Wirkung und Nebenwirkung, Zusammensetzung und erforderlichen Adjuvanzien, untersucht.
Bei der CoVid-Impfstoffentwicklung konnte man auf vorausgehende Untersuchungen zu anderen RNA-Impfstoffen zurückgreifen (MERS, SARS, Ebola).
Klinische Phasen
Grundsätze der klinischen Phasen
An die Präklinische Phase schließen sich die klinischen Phasen an, in denen der Impfstoff am Menschen untersucht wird.
Insbesondere an die ersten Phasen der Testungen (Phase I – III) werden hohe Anforderungen gestellt. Sie müssen von der Ethikkommission genehmigt werden. Der Goldstandard sind randomisierte doppel-verblindete kontrollierte Studien. Die Versuchsteilnehmer werden per Zufall in zwei Gruppen aufgeteilt, wer welcher Gruppe angehört wissen weder die Versuchsteilnehmer noch die Versuchsdurchführenden. Eine Gruppe erhält die Impfung, die zweite Gruppe ein Placebo, also eine harmlose und unwirksame „Impfung“. Hierdurch können Wirkungen und Nebenwirkungen ermittelt werden.
Sowohl in der Wirkstoff-Gruppe als auch in der Placebo-Gruppe können für die Teilnehmer der Studie erhöhte Risiken bestehen: In der klinischen Phase der CoVid-19-Impfstoffe verstarb 1 Person aus der Placebo-Gruppe an Corona (keine aus der Wirkstoff-Gruppe). Auch bei den COVID-19-Erkrankungen und den schweren COVID-19-Erkrankungen waren die Teilnehmer der Placebogruppe stärker betroffen (s. unten).
Beispiel für negative Wirkungen in der Wirkstoff-Gruppe siehe nachfolgenden Abschnitt.
Phase I: Proof of Principle
An einer kleinen Gruppe Freiwilliger (30 – 50 Personen) wird der Wirkstoff zum ersten Mal an Menschen getestet. Ziel dieser Untersuchungen ist es u. a., die vermuteten Eigenschaften auch beim Menschen zu verifizieren und erste Erkenntnisse zu Sicherheit und Verträglichkeit zu erhalten.
Selbst bei Auswahl des richtigen „Tiermodells“ in der Präklinischen Phase ist eine Übertragung der Ergebnisse auf den Menschen nicht immer 1:1 möglich. Im Gegensatz zu Medikamenten steigt die Wirkung von Impfstoffen nicht linear mit der Dosis an, sondern erfolgt erst ab einer bestimmten Dosis. Hierdurch wird die Dosisfindung durch Übertragung der Ergebnisse aus der Präklinischen Phase zusätzlich erschwert.
Beispiel „Übertragungsfehler“: Das Medikament TGN1412 sollte zur Behandlung von verschiedenen Autoimmunerkrankungen eingesetzt werden. In der Phase I der Studien überreagierte das Immunsystem der 6 Testpersonen, sie zeigten Anzeichen eines akuten Schocks. Alle Teilnehmer überlebten, behielten jedoch teilweise irreversible Schäden. Die aus den Tierversuchen abgeschätzte Dosis war in diesem Fall zu hoch.
Die Ergebnisse dieser Phase stellen die Basis für die weiteren Untersuchungs-Phasen dar.
Phase II: Dosisfindung
Auch bei dieser Phase geht es u. a. um Sicherheit, Verträglichkeit, Wirkung und Nebenwirkung, aber auch um das Optimieren der Dosis.
An dieser Phase nehmen üblicherweise 200 – 400 Personen teil.
Phase III: Zulassungsstudie
Nach erfolgreicher Durchführung der vorherigen Phasen wird die Anzahl der Testpersonen ausgeweitet auf 3.000 – 10.000 Personen. Aufgrund der höheren Personenzahl können Aussagen zu Wechselwirkungen, Impfversagen sowie zu Kosten, Risiko und Nutzen getroffen werden.
Seltene Nebenwirkungen (weniger als ca. 1:10.000) und deren ggf. langfristigen Folgen können aufgrund der Anzahl der Testpersonen jedoch nicht sicher ermittelt werden.
Auf Basis der gewonnenen Erkenntnisse kann der Zulassungsantrag gestellt werden.
| Hersteller | BioNTech Manufacturing GmbH | MODERNA BIOTECH SPAIN, S.L. | AstraZeneka | Janssen-Cilag International |
|---|---|---|---|---|
| Studienteilnehmer | 43.548 | 30.420 | 12.196 | 44.325 |
| Erkrankte | Nicht Erkrankte | Gesamt | |
|---|---|---|---|
| Geimpfte | 0,0689 % | 50,0134 % | 50,0823 % |
| Ungeimpfte | 0,3371 % | 49,5801 % | 49,9172 % |
| Gesamt | 0,406 % | 99,5940 % | 100 % |
Der Anteil der Erkrankten ist bei den Studien sehr gering. Allerdings ist dabei zu berücksichtigen:
- Alle Teilnehmer unterlagen den mehr oder weniger strengen Schutzmaßnahmen während der Lock-Down-Phasen.
- Da die Teilnahme freiwillig war, ist davon auszugehen, dass seitens der Studienteilnehmer ein Problembewusstsein vorhanden war und z. B. Schutzmaßnahmen konsequent eingehalten wurden.
Es ist davon auszugehen, dass sich das Verhältnis erkrankt / nicht erkrankt in der Gesamtbevölkerung anders darstellt.
Aus den Unterschieden zwischen Wirkgruppe und Kontrollgruppe ergibt sich die Wirksamkeit der Impfstoffe. Die Impfungen können die Wahrscheinlichkeit an COVID -19 zu erkranken deutlich senken, die Wahrscheinlichkeit einer schweren COVID-19-Erkrankung ist drastisch gesenkt.
Zulassung
Im Zulassungsverfahren wird u. a. die Sicherheit des Impfstoffes bewertet. Die Prüfung beginnt üblicherweise nach einreichen aller erforderlichen Unterlagen und dauert zwischen einem halben und einem 3/4 Jahr.
In Deutschland ist das Paul-Ehrlich-Institut (PEI, Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel) für die Erteilung von Zulassungen zuständig.
Basis der Zulassungsentscheidung sind Risiko-Nutzungsabwägungen (epidemiologischen Risiko-Nutzen-Abwägung). Es wird überprüft, ob der Impfstoff sicher und wirksam ist. Die Wirksamkeit muss deutlich über dem Risiko (u. a. Nebenwirkungen) liegen. Da der Einsatz von Impfstoffen nicht kurativ (behandelnd) sondern präventiv (vorbeugend) ist, werden höhere Anforderungen an das Verhältnis Wirkung zu Nebenwirkung (bzw. allgemein: Nutzen zu Kosten) gestellt.
Wichtige Aspekte der Zulassung sind u. a.:
- Sicherheit des Impfstoffes
- Wirksamkeit
- Qualität des Impfstoffes (Hinweis: auch nach der Zulassung muss bei Impfstoffen jede Charge geprüft werden)
- Nutzen-Risiko-Verhältnis.
| COVID-19-Erkrankungen bei Ungeimpften (Bezug: Bevölkerung) | Nebenwirkungen bei Geimpften (Bezug: Geimpfte) | |
|---|---|---|
| Schwere COVID-19-Erkrankung bzw. schwere Nebenwirkungen durch Impfung | 7,50 % | 0,17 % Meldungen 0,02 % schwere Nebenwirkungen |
| Tod durch COVID-19 bzw. durch Impfung | 2,80 % | 0,0019 % |
| Langzeitwirkungen | Vorhanden, aber Anteil nicht sicher bekannt | Unbekannt, aber unwahrscheinlich; Nebenwirkungen mit langfristigen Folgen möglich |

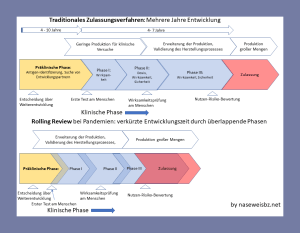
Die „bürokratischen Hürden“ bei den Studien und der Zulassung (also die Anforderung, sich strikte an die vorgegebenen Abläufe und Durchführung von Studien zu halten), verzögern eine schnelle Entwicklung. Das stößt und stieß zum Teil bei Betroffenen, z. B. Krebspatienten, HIV-Kranke, auf Unverständnis.
Die EMA (Europäische Arzneimittel-Agentur) hat für zeitkritische Zulassungen (z. B. während einer Pandemie) vom regulären Verfahren abweichende Prozesse vorgesehen, die eine schnelle, aber dennoch sichere Herstellung und Zulassung gewährleisten sollen.
Bei den COVID-19-Impfstoffen wurde für Entwicklung und Zulassung das Verfahren des Rolling Review eingesetzt:
- Die einzelnen Phasen wurden soweit möglich zeitlich überlappend durchgeführt. Erleichtert wurde dies u. a. durch die finanziellen Zuschüsse an die Herstellerfirmen.
- Die Zulassungsgrundlagen wurden nicht gebündelt nach Abschluss aller Studien mit der Zulassung eingereicht, sondern schon vor Ende der Studien zur Prüfung an die Zulassungsstellen übermittelt.
- Einige Unterlagen liegen zum Zeitpunkt der Zulassung noch nicht (final) vor. An die Zulassung ist die Anforderung gekoppelt, noch fehlende (unvollständige) Unterlagen bis zu jeweils vorgegebenen Zeitpunkten nachzureichen.
Insgesamt ergibt sich dadurch eine erhebliche Verkürzung der Entwicklungs- und Zulassungszeit bei nahezu gleichen Anforderungen.
Bei der Zulassung wird u. a. ein Risikomanagement-Plan vorgegeben, der die weitere Überwachung der Impfsubstanz festschreibt.
Home // Seitenanfang // Alle Beiträge Naturwissenschaft
Phase IV: Postmarketing-Studie
Nach der (zunächst auf 5 Jahre befristeten) Zulassung erfolgt die Vermarktung des Impfstoffes. Die Erfahrungen mit dem breiten Einsatz des Impfstoffes werden kontinuierlich überwacht und ausgewertet.
Aufgrund der hohen Anzahl an Geimpften können auch sehr seltene Nebenwirkungen erkannt werden. Bei Verdacht auf über das übliche Maß hinausgehende Nebenwirkungen sind diese nach § 6 Abs. 1 Infektionsschutzgesetz (IfSG) meldepflichtig. Zusätzlich können alle Verdachtsfälle von Nebenwirkungen direkt an die Hersteller oder das PEI gemeldet werden.
In Zusammenhang mit den CoVid-19-Impfungen wurden insgesamt 49.442 Verdachtsfälle gemeldet (entspricht 0,17 % in Bezug auf alle Impfungen) ([1], Stand: 29.04.2021). Allerdings muss nicht jeder gemeldete Verdachtsfall einen tatsächlichen Bezug zur Impfung haben. Zum Zeitpunkt der Meldungen waren 40,1 % der unerwünschten Reaktionen bereits vollständig abgeklungen.
Bei einem Großteil der Verdachtsfälle handelt es sich um „leichte“ (nicht schwerwiegende) Verdachtsfälle, wie z. B. Ausschlag, Schwellungen und / oder Schmerzen an der Injektionsstelle, Gliederbeschwerden, Unwohlsein, grippeähnliche Erkrankungen, Ermüdung. Hierbei handelt es sich um häufig bei Impfungen festgestellte Symptome bzw. zu erwartende Symptome.
Von den gemeldeten Verdachtsfällen wurden 0,2 Fälle je 1.000 Impfdosen als schwerwiegende Reaktionen eingestuft (also bei 0,02 % der Impfdosen) (s. auch Tabelle oben). Tod bzw. bleibende Schäden wurden bei 1,1 % bzw. 0,6 % der Verdachtsfälle gemeldet (entspricht rd. 550 Tote bzw. rd. 300 Fälle mit bleibenden Schäden). Bezogen auf alle Impfungen entspricht das 0,0019 bzw. 0,001 % (Summe: rd. 0,003 %).
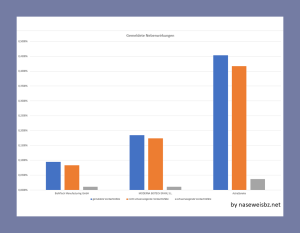
Im Universitätsklinikum Schleswig-Holstein wurden die Krankschreibungen nach den Impfungen untersucht. Der Impfstoff von Janssen war zu diesem Zeitpunkt noch nicht zugelassen, es waren noch keine Zweitimpfungen mit AstraZeneka erfolgt.
Nach Erstimpfung mit AstraZeneka waren 65,3 % einen oder mehrere Tage arbeitsunfähig (der größte Teil betraf ein oder zwei Tage Arbeitsunfähigkeit). Bei Moderna und BioNTech traten Krankschreibungen eher nach der zweiten Impfung auf, waren aber bei beiden Impfschritten insgesamt geringer als bei AstraZeneka. Bei Moderna traten viele Krankschreibungen nach der 2-ten Impfung auf.
Werden in dieser Phase bisher nicht festgestellte (schwere) Nebenwirkungen festgestellt (oder die festgestellten Nebenwirkungen treten häufiger als erwartet auf), wird die Zulassung ggf. zurückgezogen oder geändert und spezielle Hinweise an Ärzte gegeben. Die neuen Erkenntnisse fließen in eine neue Produktbewertung ein.
Beispiel: Rote-Hand-Brief zur COVID-19-Vakzine von AstraZeneca der gelben Liste
Die festgestellten Erkenntnisse werden vom PEI veröffentlicht (Sicherheitsbericht) und sind öffentlich einsehbar.
Beispiele: Veröffentlichung des PEI:
Des Weiteren wird in dieser Phase u. a. auch getestet, ob die vermutete Impfeffektivität erreicht wird.
Gegebenenfalls können noch weitere Studien erforderlich sein, z. B. hinsichtlich der Dauer des Impfschutzes, auftreten indirekter Effekte oder zur Impfsicherheit bei besonderen Personengruppen.
Impfempfehlung
Die STIKO erteilt Impfempfehlungen und fasst wichtige Impfungen in Impfplänen zusammen. Die Impfstoffe werden neben der epidemiologischen Sicht auch aus gesundheitsökonomischer Sicht bewertet.
Bei der Entscheidung, einen Impfstoff in einen Impfplan aufzunehmen sind zahlreiche Kriterien relevant, z. B.
- Sicherheit und Wirksamkeit des verfügbaren Impfstoffs,
- schwere der Erkrankung und lokale Epidemiologie (z. B. Inzidenz / Schwere allgemein und in bestimmten Alters- bzw. Risikogruppen),
- erwartete indirekte Effekte (positive und negative),
- Integration in Impfkalender: ab welchem Alter und in welchen Abständen,
- Kosten-Effektivität, z. B. hinsichtlich Kosten von Impfkampagnen, Aufklärung.
Es werden verschiedene Modellrechnungen durchgeführt, mit denen vermiedene Krankheitsfälle, Todesfälle, Krankenhausaufenthalte oder auch gewonnene Lebensjahre und Qualität der Lebensjahre (englisch: QALY) abgeschätzt werden. Die direkten und indirekten Krankheitskosten werden dem individuellen und gesellschaftlichen Nutzen einer Impfung gegenübergestellt.
In Bezug auf CoVid-19 wurden somit bei der Impfempfehlung auch Verfügbarkeit von Intensivbetten, wirtschaftliche und individuelle Folgen des Lockdowns, Einschränkung von Persönlichkeitsrechten und vieles mehr berücksichtigt.
Überblick der wichtigsten Akteure
Bei der Bewertung von Impfungen agieren verschiedene Institutionen zusammen, die sich jeweils aus fachlich kompetenten Wissenschaftlern zusammensetzen. Bei Bedarf können zusätzlich Expertisen eingeholt werden.
In der Grafik sind die wichtigsten Institutionen und ihr Zusammenwirken dargestellt.
RKI: beschreibt den Erreger, die Krankheit und das Risiko
PEI: erteilt nach Prüfung der Antragsunterlagen die Zulassung (oder auch nicht)
STIKO: spricht auf Basis der Zulassungsinformationen Impfempfehlungen aus
Ethikkommission: zustimmende Bewertung vor Versuchsbeginn, Zuständigkeiten für Bundesland, ZEKO: Zentrale Ethikkommission der Bundesärztekammer
Fazit:
Bei den Entwicklungen und den Zulassungen der COVID-19-Impfungen wurden keine Sicherheitsrisiken zugunsten einer schnellen Impfstoffentwicklung in Kauf genommen. Allerdings wurde durch finanzielle Zuschüsse und Optimierung der Abläufe eine kürze Entwicklungszeit möglich. Hersteller konnten auch auf vorhandene Vorarbeiten zurückgreifen. Bei der Zulassung wird u. a. der Nutzen einer Impfung gegen deren Risiko abgewogen. Nach der Zulassung wird der Impfstoff nach einem vorgegebenen Plan intensiv überwacht und bei Bedarf die Zulassung angepasst.
Quellen (Daten und Zitate, in der Reihenfolge der Erwähnung)
- PEI: Coronavirus und COVID-19: Sicherheitsbericht 27.12.2020 bis 30.04.2021
- Oberle D et al.: Fall-Kontroll-Studie zu Risikofaktoren von Narkolepsie in Deutschland. Somnologie-Schlafforschung und Schlafmedizin 1·2013
- Impf-Info: COVID-19, die Impfungen und die Herde, 30.04.2021 – Herdenimmunität durch CoVid-19-Impfstoffe – AstraZeneka
- Wiedermann U, Kistner O, Tucek B: Entwicklung von Impfstoffen, OÄZ 23/ 24, 15. Dezember 2017 DFP 2017
- RKI: Epidemiologisches Bulletin 16/21: Beschluss der STIKO zur 4. Aktualisierung der COVID-19-Impfempfehlung und die dazugehörige wissenschaftliche Begründung
- Lurie N, Saville M, Hatchett R, Halton J: Developing Covid-19 Vaccines at Pandemic Speed. The New England Journal of Medicine, med 382;21 nejm.org May 21, 2020
Home // Seitenanfang // Alle Beiträge Naturwissenschaft
Informationsmöglichkeiten
Impfgeschehen
Verimpfte Dosen auf dem Impfdashboard
Aktueller Impfstatus, Impfdashboard
Fragen zur COVID-19-Impfempfehlung, RKI
Informationen zu den Impfstoffen
Produktinformationen Übersicht, PEI, verlinkt auf EMA
Vergleich der Corona-Impfstoffe, Gelbe Liste
Unterschiede der Corona-Impfstoffe, Gelbe Liste
Die vier Corona-Impfstoffe im Vergleich. Apotheker Rundschau, 03.05.2021
Impfstoffe, BMG – Impfstoffe, Entwicklung und Zulassung, Wirksamkeit und Sicherheit, CoVid-19-Impfstoffe
Corona-Schutzimpfung gegen COVID-19, Infektionsschutz.de
COVID-19 und Impfen: Antworten auf häufig gestellte Fragen (FAQ), RKI
Coronavirus – Aktuelle Informationen, PEI – z. B. Aufklärungsbögen zu den Impfungen, FAQs, Impfmonitoring, Fallzahlen
mRNA-Impfstoffe
mRNA als neues Impfstoffprinzip, Pharmazeutische Zeitung 02 / 2021
mRNA-Impfstoffe, BioNTech
Aufklärungsbogen RKI zu mRNA-Impfstoffen
Vektorimpfstoffe
Vektorviren als Plattform, Pharmazeutische Zeitung, 07 / 2020
Ich habe eine Frage zum Impfen: (Auswirkung auf Erbgut). Impfen-info.de BZgA
Aufklärungsbogen RKI zu Vektorimpfstoffen
Impfstoffe allgemein
Das sollten Sie über Impfstoffe wissen, BMBF
Sicherheit der Impfstoffe
Sicherheit von CoVid-19-Impfstoffen, PEI
Wie sicher sind die Corona-Impfstoffe?, SR
Nebenwirkungen der Impfstoffe
Allgemein: Reaktionen und Nebenwirkungen nach Impfungen, Institut für Spezifische Prophylaxe und Tropenmedizin der MedUni Wien, 2013 – sehr guter Überblick über Nebenwirkungen von Impfungen – Erläuterungen und Definitionen in Ergänzung zum Österreichischen Impfplan.
Grafische Auswertung europaweiter Nebenwirkungen, EMA
Warum es keine Langzeit-Nebenwirkungen gibt. ZDF
Welche Langzeitfolgen zu befürchten sind, Pharmazeutische Zeitung Februar 2021
Impfstoffentwicklung, -zulassung und -empfehlung
Impfstoffentwicklung und -zulassung, infektionsschutz.de – BZgA
Mit welchen Technologien werden Impfstoffe gegen Viren entwickelt?, infektionsschutz.de – BZgA
by naseweisbz.net



