B. Bassler und M. Silvermann erhalten den Paul-Ehrlich-Preis für ihre Forschungen zur Kommunikation von Bakterien, die neue Ansätze für Therapien ermöglichen. Dass Bakterien miteinander und anderen Lebewesen kommunizieren, ist schon länger bekannt.
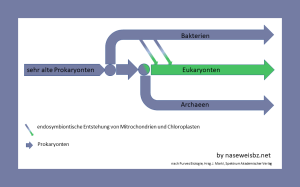
Zum besseren Verständnis sehr stark vereinfacht
Bakterien
Lebewesen werden in 3 Domänen eingestuft: Bakterien, Archaeen und Eukaryonten.
Die Archaeen sind Einzeller, die häufig in extremen Standorten vorkommen. Sie unterscheiden sich von den beiden anderen Domänen u. a. durch ihren deutlich anderen Zellwandaufbau.
Bei Eukaryonten ist der Zellkern von einer Membran umgeben, ebenso wie meist die Organellen („Organe“ der Zelle, z. B. für die Energiegewinnung). Diese Domäne enthält sowohl Einzeller als auch Vielzeller. Hierzu zählen Menschen, Tiere und Pflanzen.
Bakterien…..
- sind wie die Archaeen Einzeller. Die häufigsten Formen sind Stäbchen, Kugeln oder Spiralen.
- sind die häufigsten Individuen auf der Erde. Alleine im Meer leben vermutlich mehr als 3X1028 Bakterien (und Archaeen) – das ist 100 Millionen Mal mehr, als Sterne im sichtbaren Universum. Die Zahl der Bakterien im und auf dem Menschen (rund 1,5 kg) übersteigt die Zahl der menschlichen Zellen um das 10-fache (ca. 1014 Bakterien auf 1013 menschliche Zellen). Allein im Darm eines Menschen leben mehr Bakterien, als jemals Menschen auf der Erde gelebt haben. Man schätzt, dass auf der Haut des Menschen mehr als 1000 Bakterienarten existieren, pro cm² Haut ca. 106 Bakterien.
- haben wichtige Funktionen im Ökosystem inne. Sie zersetzen z. B. Substanzen und spielen daher eine wichtige Rolle im Stoffkreislauf. Aber auch in und auf Vielzellern sind sie als Freund und Feind relevant.
- sind im Darm des Menschen als Symbionten aktiv und liefern dem Menschen – als Abfallprodukte ihres Stoffwechsels – z. B. Vitamin B12 und Vitamin K. Die Zusammensetzung des Biotops „Bakterien“ variiert von Mensch zu Mensch und kann sich auch beim einzelnen Menschen zeitweise verändern, z. B. in Abhängigkeit von Ernährung oder Medikamenteneinnahme.
Im Pansen von Wiederkäuern sind Bakterien für die Zersetzung der Zellulose verantwortlich, die den Wiederkäuern eine Ernährung durch Gras ermöglicht. - übernehmen auf der Haut eine wichtige Schutzfunktion, indem sie anderen Bakterien keinen Platz lassen bzw. aktiv gegen diese vorgehen. Das Immunsystem des Körpers muss daher zwischen einer erwünschten Bakterien-Besiedlung der Haut und unerwünschten Bakterien unterscheiden können.
Von den zahlreichen existierenden Bakterien sind nur wenige krankheitserregend (pathogen): Im Laufe der Evolution hat sich ein Miteinander entwickelt.
Gemeinsam sind wir stark – Quorum Sensing
Kommunikation
Bakterien kommunizieren, um für sich günstige Lebensbedingungen zu realisieren. Mit der Kommunikation können sie sich an Bakterien der eigenen Art, andere Bakterien / Einzeller, aber auch an höhere Lebewesen richten.
Die Kommunikation der Bakterien wird als Quorum Sensing (QS) bezeichnet. Durch die innerartliche Kommunikation werden Aktionen koordiniert.
Analog wie beim Menschen zeichnet sich die Sprache der Bakterien aus durch:
- geringe Kosten: für die Produktion der verwendeten Signale ist nur wenig Energie erforderlich, z. B. werden als Signalstoffe teilweise Abfallprodukte des Stoffwechsels verwendet.
- Abgrenzung von Gruppen: verschiedene Bakterien benutzen unterschiedliche Signalmoleküle.
- Lenkung des Gruppenverhaltens; Kommunikation ermöglicht es, gemeinsam ein Ziel zu erreichen, das ein Einzelner nicht erreichen kann.
Verschiedene Verhaltensweisen erfordern einen unterschiedlichen Energieeinsatz, der über die Gruppe durch die Kommunikation optimiert wird. Manche Einzel-Aktivitäten eines Bakteriums „lohnen“ sich erst ab einer bestimmten Menge von Bakterien, die sich gleich verhalten.
Das wesentliche Entscheidungskriterium für den Beginn einer gemeinsamen Aktion ist daher die Feststellung der Bakteriendichte.
Durch die Koordination von gemeinsamen Aktivitäten können verschiedene Ziele erreicht werden, z. B.
- Biolumineszenz,
- Bildung von Biofilmen,
- Bildung extrazellulärer Enzyme und Virulenzfaktoren,
- Endosporenbildung,
- DNA-Austausch.
Home // Seitenanfang // Alle Beiträge Naturwissenschaft
Die Sprache der Bakterien
Von den Bakterien werden verschiedene Signale und Signalstoffe (mindestens 20 sind derzeit bekannt) verwendet. Diese Signale sind z. T. artspezifisch, können also nur von Bakterien der gleichen Art „verstanden“ werden, zum Teil artübergreifend, sind also „allgemeinverständlich“.
Vorwiegend werden chemische Substanzen benutzt, es kommen aber auch physikalische Signale (Licht, Elektrizität) zum Einsatz.
Die Signalstoffe werden über Rezeptoren in der Zellwand „wahrgenommen“. Fehlt der entsprechende Rezeptor, bleibt das Bakterium „taub“ gegenüber dem Signal. Sind alle Rezeptoren bereits besetzt, z. B. durch eine chemisch ähnliche Substanz, kann das Signal ebenfalls nicht wahrgenommen werden.
Die chemischen Signalstoffe sind Autoinduktoren (AI), da nach Aufnahme eines Signalmoleküls die Produktion von eigenen Signalmolekülen aktiviert wird (positive Rückkopplung).
Die Rezeptoren leiten das Signal in die Bakterienzelle weiter. Dort werden bestimmte Gene aktiviert (Genexpression), wodurch die Bildung der entsprechenden Proteine, z. B. Enzyme, erfolgt. Durch unterschiedliche Proteine werden unterschiedliche Stoffwechselvorgänge realisiert, die unterschiedliche Verhaltensweisen oder Phänotypen der Bakterien bewirken. Es handelt sich also um einen epigenetischen Effekt: je nach „Input“ werden verschiedene Genabschnitte abgelesen. Die Umweltbedingungen haben Einfluss auf die Genexpression.
Manchmal sind für bestimmte Reaktionen der Bakterien verschiedene Signalsubstanzen erforderlich. Die Konzentration der einzelnen Signalsubstanzen wird bewertet und in Abhängigkeit vom Ergebnis verschiedene Stoffwechselwege aktiviert. So kann es z. B. sein, dass Signal B das entscheidende Signal für eine Reaktion ist, diese aber erst eingeleitet wird, wenn auch die erforderliche Konzentration von Substanz A erreicht wird (oder alternativ eine bestimmte Konzentration von Substanz A nicht überschritten wird).
Das genaue Zusammenspiel der einzelnen Signalsubstanzen, ihre Wirkung in der Zelle und die Genaktivierung sind Gegenstand zahlreicher Forschungen.
Besonders gut ist die Kommunikation bei der Bakteriengattung Vibrio untersucht, die als Modellbakterium zur Erforschung von QS dient.
Gemeinsame Ziele
Biolumineszenz
Bakterien der Gattung Vibrio sind in der Lage Biolumineszenz (Licht) zu erzeugen. Die Biolumineszenz wird jedoch nur gezeigt, wenn eine bestimmte Zellzahl überschritten ist.
Ein Vertreter der Gattung Vibrio kommt zwar auch frei im Meer vor, lebt aber eigentlich im Darm von Fischen. Wird das Bakterium mit Verdauungsprodukten ausgeschieden, ernährt und vermehrt es sich weiter. Ab einer bestimmten Bakteriendichte (und Abnahme der Nahrungsbasis) wird Biolumineszenz ausgesendet, durch die Fische angelockt werden. Diese nehmen die Bakterien samt Substrat auf. Die Bakterien gelangen so in einen neuen Wirt, in dem sie ein verbessertes Nahrungsangebot finden.
Die Biolumineszenz macht sich der Zwergtintenfisch (Euprymna scolopes) zu nutze. Der nachtaktive Tintenfisch verfügt über ein Leuchtorgan, welches in flachen Gewässern dazu dient, die Kontraste zu verringern und ihn „unsichtbar“ zu machen. Im Leuchtorgan ist das Bakterium Vibrio fischeri angesiedelt. Um das Leuchten zu erzeugen, versorgt der Tintenfisch die Bakterien mit Nährstoffen, die Bakterien vermehren sich und senden ab einer bestimmten Bakteriendichte Licht aus. Am Morgen scheidet der Tintenfisch Bakterien aus dem Leuchtorgan aus, so dass die Bakteriendichte reduziert wird und die Biolumineszenz beendet wird.
Biofilm
Viele Bakterien organisieren sich in Biofilmen, die eine koordinierte Ansammlung von Bakterien darstellen. Biofilme schaffen günstigere Bedingungen für die Bakterien, weil sie andere Eigenschaften haben, als eine Ansammlung „freier“ Bakterien, z. B.:
- Die mechanische Beständigkeit des Biofilms ist sehr hoch.
- Durch eine umgebende Matrix, ist der Biofilm besser gegen Antibiotika und andere chemische Einflüsse von außen geschützt,
- Im Biofilm werden Wasser und Nährstoffe zurückgehalten, so dass ein Schutz vor Austrocknung und Hungerperioden besteht. Zusätzlich können organische und anorganische Substanzen besser im Biofilm aufgenommen werden.
- Ausgeschiedene Makromoleküle werden im Biofilm gehalten und können als zusätzliche Nährstoffe dienen.
- Durch die hohe Dichte an Bakterien kann DNA einfacher zwischen den Bakterien ausgetauscht werden. So können sich z. B. Informationen zu Antibiotika-Resistenzen im Biofilm schnell verbreiten.
- Teilweise werden weitere Mikroorganismen in den Biofilm integriert, die zu zusätzlichen positiven Eigenschaften führen können.
Home // Seitenanfang // Alle Beiträge Naturwissenschaft
Beispiele für Biofilme sind:
- Zahnbelag / Plaque,
- Beläge auf technischen und medizinischen Geräten, wie Pumpen, Kontaktlinsen, künstlichen Gelenken, Herzschrittmacher, Katheter u. v. m.
- Bei Mukoviszidose können Biofilme von Pseudomonas aeruginosa zu schwer behandelbaren und wiederkehrenden Lungenentzündungen führen.
- Im Darm des Menschen befindet sich ein Biofilm aus nützlichen Bakterien: Die dort lebenden Bakterien (und Archaeen) helfen bei der Nahrungsverwertung, ermöglichen den Übergang der Nährstoffe vom Darm ins Blut und verleihen dem Darm Immunität.
- Gesteinsbildende Cyanobakterien in stark salzhaltigen Gewässern sind für Stromatolithen verantwortlich. In der jeweils obersten Schicht existieren lebende Bakterien, wohingegen die unteren Schichten aus abgestorbenen Bakterien und Kalk bestehen.
Durch Signalstoffe können weitere Bakterien der gleichen Art, anderer Arten oder sogar eukaryontische Einzeller angelockt und integriert werden.
Beispiel: Verwendung von Elektrizität
In den Biofilmen haben die Bakterien am Rande einen besseren Zugang zu Nährstoffen, als die Bakterien im Inneren. Damit auch die Bakterien im Inneren Nährstoffe erhalten, stellen die Bakterien am Außenrand ab einer bestimmten Biofilmstärke ihr Wachstum (und ihre Vermehrung) zeitweise ein und lassen Nährstoffe ins Innere passieren.
Die Koordination kann über elektrische Potentiale in Ionenkanälen erfolgen, die an die Reizweiterleitung im Nervensystem höherer Lebewesen erinnert: Die Spannungsübertragung findet im Wesentlichen mittels Kaliumionen statt, die in Ionenkanälen durch den Biofilm wandern und zu unterschiedlichen Membranpotentialen der Zellwände führen. Die elektrische Spannung an den Zellmembranen schwankt synchron mit dem Wachsen des Biofilms. Durch die unterschiedlichen Membranpotentiale wird das Wachstum der inneren und äußeren Zellen koordiniert.
Vibrio harveji: Arbeitsteilung durch 3-1-Rezeptor-Kaskade
Vibrio harveyi kann sowohl Biofilme ausbilden, als auch Biolumineszenz erzeugen.
Das Bakterium verfügt in seiner Zellmembran über 3 verschiedene Rezeptoren, an denen verschiedene Signalmoleküle andocken können:
- Al-1 (HAl-1) ist ein artspezifisches Signalmolekül: Es dient ausschließlich der innerartlichen Kommunikation von V. harveyi.
- Al-2 kann von verschiedenen Bakterien gebildet und „verstanden“ werden.
- CAl-1 ist ein Vibrio-spezifisches Signalmolekül (ist für alle Vibrio-Bakterien „verständlich“).
Die 3 Signalmoleküle sind im natürlichen Umfeld in verschiedenen Konzentrationen vorhanden. Je nach Summe der „Signalstärke“ der 3 Signalmoleküle sind verschiedene Reaktionen in der Bakteriengruppe möglich:
- Alle drei Signalmoleküle sind in der erforderlichen Menge vorhanden: alle Zellen zeigen Biolumineszenz = es erfolgt eine einheitliche Reaktion (phänotypisch homologe Reaktion).
- Nur ein oder zwei der Signalmoleküle sind in der erforderlichen Menge vorhanden: nur einige Zellen zeigen Biolumineszenz = es erfolgt eine unterschiedliche Reaktion der Bakterien (phänotypisch heterologe Reaktion).
- Keines der drei Signalmoleküle ist in der erforderlichen Menge vorhanden: keine Zelle zeigt Biolumineszenz = es erfolgt eine einheitliche Reaktion (phänotypisch homologe Reaktion).
Durch die „differenzierte“ Auswertung von 3 Signalen ist eine effiziente Arbeitsteilung (Biolumineszenz, Biofilmbildung) möglich.
Vibrio cholerae: Aufbruch zu neuen Ufern
Die Forschungen von B. Bassler und ihrem Team beschäftigen sich mit dem QS-System von Vibrio cholerae, dem Erreger der Durchfallerkrankung Cholera.
Das Bakterium verfügt über verschiedene QS-Systeme, über die unter anderem die Virulenz und die Bildung von Biofilmen koordiniert werden.
Mittels eines speziellen QS-Systems prüft V. cholerae, ob unter den gegebenen Umständen die Ansiedlung in einem Biofilm oder eine Ausbreitung effizient ist.
Hierzu werden zwei Signalsubstanzen verwendet:
- CAl-1 prüft die Häufigkeit von Vibrio in der Umgebung
- Al-2, welches von vielen Bakterien verwendet wird, prüft das Vorhandensein anderer Bakterien.
Beide Signale müssen vorhanden sein und bilden zusammen einen Koinzidenzdetektor, über den die Bakteriendichte im Milieu ermittelt wird. Die Signale der Vibrio Gemeinschaft werden über die CAl-1-Signale quasi herausgerechnet.
Bei einer hohen Bakteriendichte löst V. cholerae den Biofilm auf (bzw. beginnt gar nicht erst mit der Biofilm-Bildung) und wandert auf der Suche nach einem weniger stark besiedelten Ort ab. In diesem Fall (und anders als bei vielen anderen Bakterien) wird QS bei V. cholerae also nicht dazu verwendet, einen Biofilm zu bilden, sondern einen Biofilm aufzulösen oder zu verhindern.
Home // Seitenanfang // Alle Beiträge Naturwissenschaft
Virulenzfaktor
Bei den krankheitserregenden Bakterien sind die Virulenzfaktoren relevant für die krankmachenden Eigenschaften. Durch die Virulenzfaktoren können Bakterien an Zellen andocken, in Zellen eindringen oder Zellen zerstören. Virulenzfaktoren können sowohl Stoffwechselprodukte als auch Strukturen der Bakterien sein. Zu den Virulenzfaktoren zählen z. B.:
- Antiphagozytosefaktoren, die verhindern, dass Bakterien von den Fresszellen (Phagozyten) des Immunsystems aufgenommen werden. Hierzu gehören z. B. Protein A (bindet das IgG der Körperabwehr und macht es wirkungslos), Koagulasen (bilden eine schleimige Matrix um Bakterien), Leukozidine (haben eine schädigende Wirkung auf die Fresszellen).
- Invasionsfaktoren, die es den Bakterien ermöglichen, sich im Gewebe auszubreiten. Beispiele sind Streptokinase (löst Fibrin auf) oder Hyaluronidasen („Spreading factor“: greift die Hyaluronsäure im Bindegewebe an).
- Endo- und Exotoxine: Endotoxine werden beim Tod der Bakterien freigesetzt. Exotoxine sind Stoffwechselprodukte, die von den Bakterien abgegeben werden und im Wirtsorganismus schädigende Wirkungen haben.
Die Bildung der Virulenzfaktoren „lohnt“ sich für Bakterien zum Teil erst dann, wenn ausreichend Bakterien vorhanden sind, um eine für die Bakterien günstige Wirkung im befallenen Organismus zu erreichen.
Die durch QS koordinierte Bildung von Virulenzfaktoren ist bei Pseudomonas aeruginosa gut untersucht. P. aeruginosa verwendet 3 verschiedene Signalmoleküle, die die Bildung verschiedener Virulenzfaktoren regulieren. Zu den Virulenzfaktoren zählen:
- Toxine, wie Exotoxin A, alkalische Proteasen, die das Eindringen des Bakteriums in Gewebe und die Zerstörung von Zellen ermöglichen,
- Exopolysaccharide (EPS), z. B. Alginate, die vor Angriffen des Immunsystems schützen,
- Adhäsionsmoleküle, z. B. Piliproteine, durch die das Anheften an Zelloberflächen und so die Biofilmbildung ermöglichen,
- Bildung von Biofilm.
Wie bei vielen Bakterien werden die Signalstoffe Las und Rhl (zwei chemisch ähnliche HSL (Homoserin Lactone)) verwendet. Zusätzlich existiert bei P. aeruginosa ein dritter Signalstoff (Pqs – Pseudomonas Quinoline Signal, 2-Heptyl-3-Hydroxy-4-Chinolon).
Die Signalverarbeitung der 3 Stoffe ist sehr komplex und mit positiven und negativen Rückkopplungen ausgestattet. Daher wird QS bei P. aeruginosa häufig auch als Netzwerk bezeichnet. Durch die Las- / Rhl-Systeme werden mehr als 300 Gene reguliert, durch Pqs über 100.
Myxococcus xanthus: Endosporenbildung
Myxococcus xanthus ist ein in Biofilmen im Boden lebendes Bakterium, welches sich von organischem Material und anderen Mikroorganismen ernährt. Seine Bewegungsgeschwindigkeit ist sehr gering.
Bei Nährstoffmangel bildet M. xanthus einen mehrzelligen Fruchtkörper aus, der zahlreiche Sporen enthält (Eine Spore ist eine widerstandsfähige Kapsel ohne normale Stoffwechselaktivität, die die DNA der Ursprungszelle enthält und bei günstigeren Bedingungen wieder aktiv wird.) Lediglich 10 – 20 % der Zellen entwickeln sich zu Sporen, die restlichen Bakterien verhungern.
Die Fruchtkörperbildung ist also nicht nur sehr energieaufwendig, sondern nimmt auch den Tod von Bakterien zugunsten der überlebenden Sporen im Fruchtkörper in Kauf. Umso wichtiger ist es, der neuen Kolonie in besseren Zeiten ideale Startbedingungen zu schaffen: Dies wird durch die große Anzahl der Sporen je Fruchtkörper realisiert.
Die Sporenbildung wird durch 2 Signalstoffe gesteuert, die sich von den üblichen Bakterien-Signalstoffen unterscheiden. Die Signalmoleküle sind nicht diffusionsfähig und zudem relativ große Proteine, die auf der Zellwand sitzen. Die Signalstoffe sind dadurch an die nahezu bewegungslosen Bakterien abgepasst.
Das A-Signal wird nach ca. 2 Std. aktiviert und misst die Anzahl der hungernden Zellen. Bei Überschreiten der kritischen Grenze wird nach ca. 6 Std. durch das C-Signal die Fruchtkörperbildung gestartet. Sie verläuft in 3 Phasen (Bildung des Fruchtkörpervorläufers, Sporenbildung, Ausreifung). In allen Phasen ist das C-Signal regulatorisch wirksam. Zudem wird kontinuierlich „überprüft“, ob die Ausgangsbedingungen (Nährstoffmangel) weiterhin bestehen oder ausreichend Nährstoffe vorhanden sind und die Fruchtkörperbildung gestoppt werden kann.
Austausch von DNA
Bakterien pflanzen sich durch Zellteilung fort, eine Durchmischung des Erbmaterials, wie bei der geschlechtlichen Fortpflanzung, findet nicht statt.
Allerdings können Bakterien ihre Erbinformationen mit anderen Bakterien austauschen und neu zusammensetzen. So können z. B. Antibiotikaresistenzen ausgetauscht werden. Die Bereitschaft zum Genaustausch wird durch Signalstoffe vermittelt.
Home // Seitenanfang // Alle Beiträge Naturwissenschaft
Sprachstörungen
Mit QS Inhibitoren (QSI, auch Quorum Quenching (QQ) oder Pathoblocker genannt) wird die Kommunikation der Bakterien behindert, indem entweder die Signale gestört oder die Aufnahme der Signale durch die Rezeptoren beeinflusst wird. Dadurch können z. B. Biofilmbildung oder die Ausbildung von Virulenzfaktoren verhindert werden.
Nahezu in allen Gruppen von Lebewesen (Prokaryonten und Eukaryonten) sind Substanzen vorhanden, die QS stören können. Häufig werden Enzyme eingesetzt, die die Signalstoffe der Bakterien verändern.
Bakterien verwenden häufig Lactonase, um die speziellen Substanzen (AHL (Acylhomoserin Lacton) und HSL (Homoserin Lacton)) der innerartlichen Kommunikation bei gram-negativen Bakterien zu beeinflussen.
Bei Pflanzen sind sekundäre Pflanzenstoffe als QQ wirksam, wie z. B. Cyanate bei Kapuzinerkresse und Meerrettich. Die Rotalge Delisea pulchra produziert halogenierte Furanone , die die AHL-Signale stören.
Bei Mäusen, Ratten und Zebrafischen verhindert Acylasedie Biofilmbildung der gram-negativen Bakterien P. putida und A. hydrophila.
Antibiotika töten Bakterien ab und sind daher sehr effektiv. Zunehmend treten jedoch Resistenzen gegen die verwendeten Antibiotika auf. Zudem sind bereits in Biofilmen angesiedelte Bakterien schwerer durch Antibiotika zu bekämpfen.
Die Beeinflussung oder Imitation von QS könnte neue Wege bei der Therapie eröffnen, indem die Ansiedlung und Biofilmbildung verhindert oder vorhandene Biofilme aufgelöst werden.
Durch Beeinflussung von QS oder Anwendung von QSI werden die vorhandenen Bakterien allerdings nicht abgetötet, sondern lediglich im Verhalten (etwa Verhinderung von Biofilmbildung) beeinflusst. Die freien Bakterien können dann jedoch entweder vom Immunsystem oder durch zusätzlich verabreichte Antibiotika angegriffen werden.
Technische Geräte, Pumpen oder Medizinprodukte könnten durch eine spezielle Beschichtung vor Biofilmbildung geschützt werden.
Bei der therapeutischen Verwendung von QSI muss sichergestellt sein, dass „erwünschte“ Biofilme, wie im Darm, nicht beeinträchtigt werden. Ein Ziel der Forschung besteht darin, detaillierte Signale und Signalverarbeitungen bei infektiösen Bakterien zu ermitteln. Hier setzen zum Beispiel die Arbeiten von Bassler / Silvermann an.
Unklar ist noch, ob Bakterien auch gegen Kommunikationsstörungen resistent werden können, z. B. indem sie neue Signalmoleküle und Rezeptoren ausbilden.
Quellen und weiterführende Literatur
Bridges AA, Bassler BL: The intragenus and interspecies quorum sensing autoinducers exert distinct control over Vibrio cholerae biofilm formation and dispersal. PLOS Biology; https://doi.org/10.1371/journal.pbio.3000429 November 11, 2019
Rasmussen T.B, Givskow M: Quorum sensing inhibitors: a bargain of effects. Microbiology (2006), 152, 895–904
Rutherfort ST, Bassler BL: Bacterial Quorum Sensing: Its role in virulence and possibilities for its control. Cold Spring Harb Perspect Med 2012;2:a012427
Sarkar K, Das RK: Review on Quorum Sensing inhibitors. IJPSR, 2019; Vol. 10(12): 5224-5233
Sogaard-Andersen L: Interzelluläre Kommunikation in Bakterien. Max-Planck-Gesellschaft – Max-Planck-Institut für terrestrische Mikrobiologie; Forschungsbericht 2004
Home // Seitenanfang // Alle Beiträge Naturwissenschaft
by maseweisbz.net